Fallbericht
Septische Kardiomyopathie oder Kounis-Syndrom? That is the question!
Fallbericht-- Ein 26-jähriger Patient stellte sich mit Verdacht auf Halsabszess vor. Seit einer Woche habe er Halsschmerzen, seit zwei Tagen eine schmerzhafte zervikale Lymphadenopathie. Dazu kommen Brustschmerz und Luftnot. Zwei Erkrankungen kommen differenzialdiagnostisch infrage. Was denken Sie?
Veröffentlicht:
Valentin Günzler Universitätsklinikum Regensburg
© Günzler
Am Folgetag berichtete der Patient plötzlich über pektanginöse Beschwerden sowie Dyspnoe. Unverzüglich abgenommene kardiale Marker zeigten sich hochpositiv sowie mit relevanter Dynamik (Abb. 1). Bei unauffälligem EKG zeigte sich echokardiografisch eine hochgradig eingeschränkte linksventrikuläre Pumpfunktion (LVEF) von 28 % bei globaler Hypokinesie und unauffälligem Koronarstatus. Bald verschlechterte sich die respiratorische Situation, sodass eine intensivmedizinische Versorgung erfolgte.
Differenzialdiagnostisch wurden eine septische Kardiomyopathie oder ein Kounis-Syndrom diskutiert.
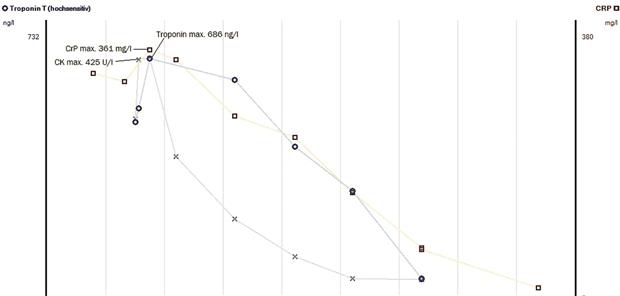
Abb. 1-- Verlauf der laborchemischen Parameter CrP (C-reaktives Protein), Troponin T und CK (Creatin Kinase) während des Aufenthalts.
© Günzler/Schach/Maier
Kounis-Syndrom charakterisiert durch Vasospasmen ausgelöstes ACS
Das aufgrund der initialen allergischen Reaktion diskutierte Kounis-Syndrom wurde 1991 erstmals beschrieben und äußert sich durch ein durch Vasospasmen ausgelöstes akutes Koronarsyndrom. Diese entstehen durch eine inflammatorische Mastzell-induzierte Reaktion des Körpers unter Beteiligung von Rezeptoren auf der Thrombozytenoberfläche[1, 2]. Induziert wird das Syndrom dabei u. a. von Medikamenten, autoimmune Prozessen und bestimmten Lebensmittel[2]. Die Therapie zielt dabei vor allem auf die Behandlung der Inflammation ab.
Septische Kardiomyopathie mit nichtischämischer Genese
Die seit den 1980er Jahren beschriebene septische Kardiomyopathie ist hingegen ein akutes, nichtischämisches Syndrom im Rahmen einer Sepsis[3], das vor allem bei jungen, männlichen Patienten beobachtet wird[4]. Ursächlich sind Entzündungsmediatoren, die begleitet von einer Proteolyse, einer mitochondrialen Schädigung, einer Stickstoffmonoxid-Dysregulation, einer verminderten β-Rezeptor-Expression sowie einer Calcium-Verschiebung eine Herzinsuffizienz induzieren[5–8]. Bei bisher fehlender spezifischer Therapie steht die Behandlung kausaler septischer Ursachen im Vordergrund.
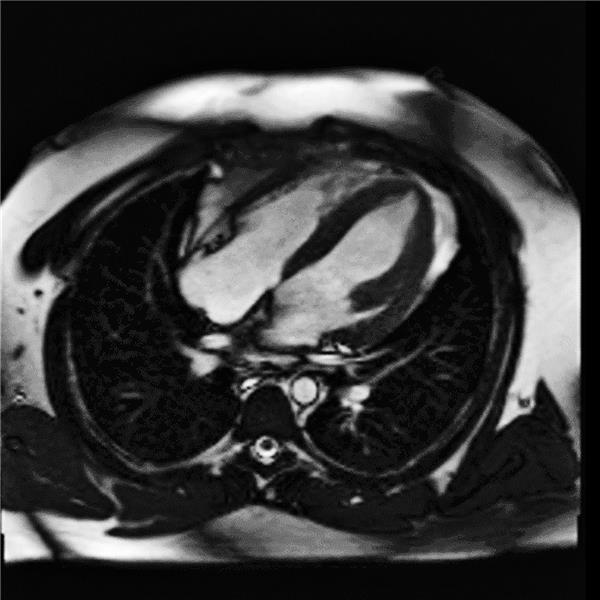
Abb. 2-- MR-Darstellung des Herzens ohne Nachweis eines Late Gadolinium Enhancement als Hinweis auf eine Myokarditis oder eines Nachweises anderer myokardialer Pathologien.
© Günzler/Schach/Maier
Ausschlussdiagnose gestellt
Zusammenfassend wurde bei diesem Patienten als Ausschlussdiagnose tatsächlich eine septische Kardiomyopathie diagnostiziert – auch weil sich bereits durch die Eskalation der antibiotischen Therapie eine deutliche Verbesserung der LVEF (auf ca, 40 %) zeigte. Zudem wurde eine Therapie mit dem Inotropikum Levosimendan durchgeführt[9].´Hierunter besserten sich sowohl der Infekt als auch die kardiale Situation des Patienten sukzessiv, sodass der Patient nach fünf Tagen auf die Normalstation verlegt und die antibiotische Therapie nach zehn Tagen beendet werden konnte.
Die Blutkulturen hatten zu keinem Zeitpunkt einen Keimnachweis ergeben und die weitere differenzialdiagnostische Abklärung im Hinblick auf (hämato-)onkologische und rheumatologische Erkrankungen oder eine toxikologische Ursache der Beschwerden war unauffällig verblieben.
Im Herz-MRT fanden sich nach Abschluss der Therapie wieder eine normale LVEF, jedoch kein Anhalt für eine Myokarditis oder andere kardiale Pathologien (Abb. 2).
Erfreulicherweise konnte der Patient die Klinik nach elf Tagen in gutem Allgemeinzustand wieder verlassen
Literatur bei den Verfassern.

