Antithrombotische Therapie nach TAVI und TEER
Update-- Vor allem ältere und komorbide Patienten mit Aortenklappenstenose oder atrioventrikulären Vitien profitieren von Herzklappen-Interventionen mit TAVI und TEER. Die Frage, „Wie und wie lange danach antithrombotisch therapieren“, beantwortet dieser Beitrag anhand der aktuellen Studienlage.
Veröffentlicht:
Je nach Patientenkollektiv kann eine SAPT, DAPT oder OAK eingesetzt werden, die Indikation ist jeweils genau zu prüfen. New Africa/stock.adobe.com
© [M] New Africa/stock.adobe.com
Für ältere Patienten mit relevanten Herzklappenerkrankungen und erhöhtem Risiko sind sowohl die TAVI (Transkatheter-Aortenklappenimplantation) bei hochgradiger Aortenklappenstenose als auch die TEER (Transkatheter-Edge-to-Edge-Reparatur) bei hochgradigen atrioventrikulären (AV) Klappenvitien etablierte Standardtherapien. Für die Nachbehandlung dieser Patienten nach Klappeninterventionen hat die antithrombotische Therapie eine besondere Bedeutung, insbesondere mit dem Ziel, ischämische und thromboembolische Ereignisse zu verhindern.

PD Dr. Claudia Walther--Cardioangiologisches Centrum Bethanien, Frankfurt/M.
© Walther

Dr. Thomas Schmitz--Contilia GmbH Essen
© Schmitz
Antithrombotische Therapie nach TAVI
Aufgrund ihres häufig fortgeschrittenen Alters haben TAVI-Patientinnen und -patienten per se ein erhöhtes thrombogenes, aber auch hämorrhagisches Risiko. Zusätzlich vorhandene Komorbiditäten wie KHK und Vorhofflimmern machen eine Thrombozytenaggregationshemmung bzw. eine dauerhafte Antikoagulation notwendig. Dieser Fakt sollte bei der Auswahl der gerinnungshemmenden Therapie berücksichtigt werden.
1. Keine Indikation zur Antikoagulation: In der randomisierten POPular-TAVI-Studie [1] konnte ein positiver Nutzen einer singulären (SAPT) gegenüber einer dualen antithrombozytären Therapie (DAPT) bzw. einer Kombination von oraler Antikoagulation (OAK) und singulärer Thrombozytenaggregationshemmung nach TAVI-Prozedur gezeigt werden. Dies ist vor allem auf eine deutlich reduzierte Blutungsneigung unter SAPT bei gleicher Wirksamkeit hinsichtlich ischämischer Ereignisse zurückzuführen. Diese Studienergebnisse wurden in den aktualisierten ESC Leitlinien von 2021 berücksichtigt [2], welche eine dauerhafte SAPT empfehlen. Bei Patienten mit Koronarintervention innerhalb der letzten 3 Monate sollte eine DAPT mit ASS und Clopidogrel für 1–3 Monate fortgeführt werden, mit anschließender ASS-Monotherapie.
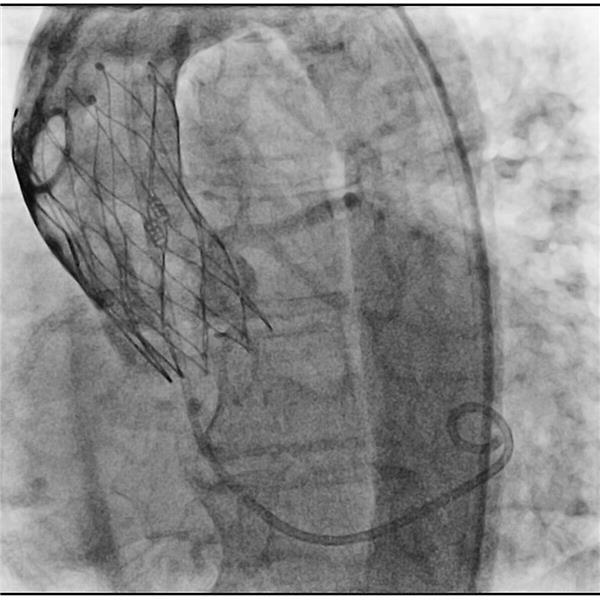
Abb. 1-- Röntgenbild einer TAVI-Implantation. Walther
© Walther
In einer aktuellen Netzwerk-Metaanalyse über 7 randomisierte Studien [3] konnte ein überlegenes Nutzen-Risiko-Verhältnis einer SAPT gegenüber einer DAPT und unterschiedlichen DOAK-Therapieformen demonstriert werden, was letztendlich die Therapieempfehlungen der Leitlinien von 2021 bestätigt.
2. Indikation zur dauerhaften Antikoagulation nach TAVI: Die ESC-Leitlinien von 2021 empfehlen die Fortführung einer dauerhaften OAK bei Patienten, die aus anderen Gründen eine Indikation zur OAK haben, allerdings gibt es keine Angabe zur Wahl des Antikoagulans.
In den beiden randomisierten Studien ENVISAGE-TAVI AF [4] und ATLANTIS [5] wurde eine DOAK-Therapie (Edoxaban und Apixaban) mit Vitamin-K-Antagonisten (VKA) verglichen. In beiden Studien wurde eine gleiche Effektivität von DOAK- und VKA-Therapie hinsichtlich der kombinierten Endpunkte von ischämischen und thromboembolischen Ereignissen beobachtet, jedoch zeigte sich unter der Therapie mit Edoxaban eine erhöhte gastrointestinale Blutungsneigung.
Insgesamt ergeben sich aus den aktuellen Studien Hinweise dafür, dass bei älteren, multimorbiden Patienten nach TAVI eine gerinnungshemmende Therapie mit DOAK sicher durchführbar ist. Für eine ausdrückliche Empfehlung ist die Datenlage noch zu ungenau, hier sind noch weitere Studien für eine bessere Evidenz notwendig.
Antithrombotische Therapie bei AV Klappeninterventionen
Randomisierte Studien zum Thema der antithrombotischen Therapie nach TEER der atrioventrikulären (AV) Klappenvitien liegen nicht vor und es gibt auch keine Empfehlungen in den europäischen Leitlinien. Die antithrombotische Therapie nach TEER ist rein empirisch und ist adaptiert an die Therapiestrategien der aktuellen publizierten Studien zur TEER bei Mitralklappeninsuffizienz [7, 8, 9].
1. Keine Indikation zur OAK: Es wird eine duale Thrombozytenaggregationshemmung mit ASS und Clopidogrel (DAPT) für 1–3 Monate, gefolgt von einer Monotherapie für insgesamt mindestens 6 Monate empfohlen, entsprechend dem in den meisten klinischen Studien praktizierten Regime.
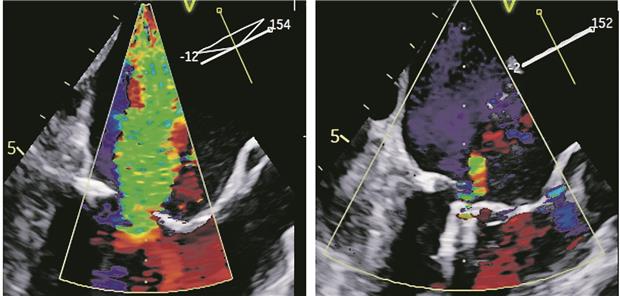
Abb. 2-- Echokardiografie der TEER der Mitralklappe, links vor der Therapie, rechts danach. Walther
© Walther
2. Indikation zur OAK: 60–70 % der Patienten, welche eine TEER erhalten, haben Vorhofflimmern und sind mit einer (D)OAK vorbehandelt. In diesem Fall sollte die vorhandene (D)OAK nach TEER weitergeführt werden. Eine zusätzliche Thrombozytenaggregationshemmung wird nicht empfohlen, denn diese würde das Blutungsrisiko weiter erhöhen und in der Folge zu einem schlechteren Outcome führen. Ausnahme von dieser Regel ist eine weitere Indikation für eine antithrombotische Therapie, wie sie eine Koronarintervention oder ein ACS darstellt. Bisher gibt es keine Daten zur Frage, welches (D)OAK in welcher Dosis angewendet werden sollte, sodass sich die Therapie an den üblichen Kriterien für eine (D)OAK-Therapie orientiert.
Die antithrombotische Therapie nach TEER der Trikuspidalklappe ist wie bei der Mitralklappeninsuffizienz anzuwenden. Der transkatheter Mitralklappenersatz sowie Valve-in-Valve-Prozeduren gehen mit einem deutlich erhöhten thrombogenem Risiko einher, sodass eine OAK in der Nachbehandlung indiziert ist – je nach Prothesenart für mindestens 3 Monate. Aufgrund der fehlenden Studienlage werden aktuell VKA empfohlen.
Insgesamt gibt es wenig Evidenz in Form randomisierter Studien hinsichtlich der antithrombotischen Therapie bei katheterinterventionellen AV Klappentherapien, sodass hier dringend weitere Studien erforderlich sind, um den Patienten eine optimale Therapie anbieten zu können.
Fazit
Bei TAVI-Patienten ohne Indikation zur OAK: dauerhafte singuläre Thrombozytenaggregationshemmung. Bei stattgehabter Koronarintervention in den letzten 3 Monaten wird eine DAPT mit ASS und Clopidogrel für 1–3 Monate empfohlen.
Bei TAVI-Patienten mit Indikation zur OAK sollte diese weitergeführt werden, DOAKs sind vergleichbar mit Vitamin-K-Antagonisten. Bei stattgehabter Koronarintervention in den letzten 3 Monaten wird eine zusätzliche Therapie mit Clopidogrel für 1–3 Monate empfohlen.
Nach TEER wird bei Patienten ohne Indikation zur OAK eine DAPT für 1–3 Monate und anschließender SAPT für insgesamt 6 Monate empfohlen.
Nach TEER wird bei Patienten mit Indikation zur OAK die Weiterführung der OAK empfohlen.
Nach katheterinterventionellem Mitralklappenersatz wird zum jetzigen Zeitpunkt eine OAK mit VKA für mindestens 3 Monate (je nach Prothesenart) empfohlen.
Kontakt-- PD Dr. Claudia Walther, MVZ CCB Frankfurt und Main-Taunus GbR, c.walther@ccb.de.
Literatur--
1. Brouwer J et al. N Engl J Med. 2020;383(15):1447-57
2. Vahanian A et al. Eur Heart J. 2022;43(7):561-632
3. Guedeney P et al Eur Heart J Cardiovasc Pharmacother. 2023;9(3):251-61
4. Van Mieghem NM et al. N Engl J Med. 2021;385(23):2150-60
5. Collet JP et al. Eur Heart J. 2022;43(29):2783-97
6. Park DW et al. Circulation. 2022;146(6):466-79
7. Stone GW et al. N Engl J Med. 2018;379(24):2307-18
8. Hochholzer W et al. Kardiologe. 2021;15:57-70
9. Waechter C et al. J Cardiovasc Dev Dis. 2022;9(11):366

