Kardiologisches Monitoring
Herzschäden durch CAR-T-Zelltherapien
Kardioonkologisches Monitoring-- Die CAR-T-Zelltherapie ist auf dem Vormarsch und könnte vielen Krebspatienten Linderung versprechen. Doch die Therapie hat einen Haken: ihr immenses kardiotoxisches Potenzial. Umso wichtiger ist eine engmaschige Überwachung der Patienten und Patientinnen.
Veröffentlicht: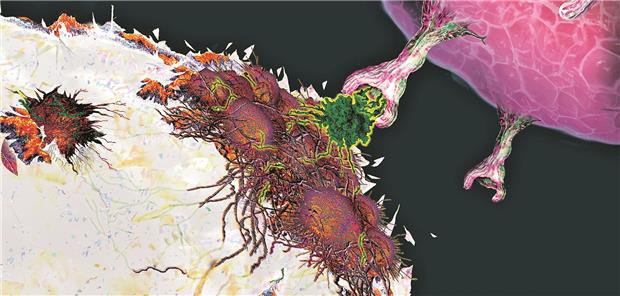
CAR-T-Zellen binden bestimmte, für Krebserkrankungen relevante Oberflächenmoleküle.
© KEITH CHAMBERS / Science Photo Library
CAR-T-Zelltherapien (CAR = chimärer Antigenrezeptor) stellen relativ neue onkologische Therapieoptionen mit hohen anfänglichen Ansprechraten für eine zunehmende Anzahl von Patienten und Patientinnen dar. CAR-T-Zellen werden vom betroffenen Patienten entnommen und richten sich nach genetischer Modifikation überwiegend gegen das Oberflächenmolekül CD19 (z. B. bei B-Zell-Akute-Lymphoblasten-Leukämie, aggressive und indolente B-Zell-Non-Hodgkin-Lymphome) und gegen Oberflächenmoleküle beim Multiplen Myelom. Es wird erwartet, dass die Indikationen für die CAR-T-Zelltherapie in den nächsten Jahren stark erweitert werden und solide Tumoren, HIV und möglicherweise kardiovaskuläre Erkrankungen umfassen könnten.

Prof. Dr. Matthias TotzeckUniversitätsklinikum Essen
© Totzeck
CAR-T-Zelltherapien können schwere allgemeine und organspezifische Toxizitäten verursachen. Das am häufigsten beobachtete unerwünschte Ereignis ist das „Cytokine Release Syndrome“ (CRS) bei bis zu 46 % der Patienten, das mit schwer beeinträchtigenden Formen und hoher Sterblichkeit auftreten kann. Über den gesamten klinischen Verlauf müssen diese Patienten engmaschig überwacht werden, und rechtzeitige Interventionen einschließlich immunmodulatorischer Medikamente (IL-6-Antagonisten und Glukokortikoide) und intensiver medizinischer Unterstützung (einschließlich kreislaufunterstützender Maßnahmen) müssen eingeleitet werden.
Erhebliche Kardiotoxizität
Auf der organspezifischen Seite der Nebenwirkungen legen neuere Daten nahe, dass die CAR-T-Zelltherapie eine erhebliche kardiovaskuläre Toxizität mit sich bringt und assoziiert werden kann mit einer erhöhten Rate an Myokardinfarkt, Arrhythmie, Herzinsuffizienz und kardiogenem Schock sowie einer Abnahme der linksventrikulären Funktion. Es kann angenommen werden, dass diese Nebenwirkungen zu einer beeinträchtigten Prognose der gefährdeten Patienten beitragen. Systematische Daten aus größeren Registern fehlen bisher allerdings.
Dem geht eine neue Arbeit aus dem European Heart Journal nach [1], die sich mit der Häufigkeit schwerwiegender kardiovaskulärer Ereignisse („severe cardiovascular events“, SCE) und der Sterblichkeit bei Empfängern von CAR-T-Zelltherapien befasst. Die Studie ergab, dass 16 % der Patienten ein SCE hatten (kombinierter Endpunkt aus Herzinsuffizienz, kardiogenem Schock oder Myokardinfarkt). Biomarker wie hochsensitives Troponin (hsTn), C-reaktives Protein (CRP), Ferritin und Interleukin-6 (IL-6) waren in der SCE-Gruppe deutlich erhöht. SCE war unabhängig mit der Gesamtsterblichkeit und der Sterblichkeit ohne Tumorrezidiv assoziiert. Die Studie ergab auch, dass Faktoren, die mit einem erhöhten Risiko für SCE verbunden sind, kardiovaskuläre Risikofaktoren wie Hypertonie sowie eine Vorgeschichte von Vorhofflimmern oder Herzinsuffizienz sind. Insgesamt zeigen diese Daten, dass CAR-T-Zelltherapien ein hohes Potenzial für kardiovaskuläre Nebenwirkungen aufweisen, gerade in Risikopatienten. Eine intensive Überwachung der Patienten ist daher empfehlenswert.
Empfehlungen der ESC-Leitlinie
Dem trägt die aktuelle Leitlinie für onkologische Kardiologie der ESC bereits Rechnung und empfiehlt: Bestimmung von natriuretischen Peptiden und hochsensitivem Troponin zusammen mit einem Elektrokardiogramm (EKG) bei allen Patienten vor der Therapie (Empfehlungsklasse IC). Bei allen Patienten mit bestehenden Herz-Kreislauf-Erkrankungen wird eine Echokardiografie empfohlen (Empfehlungsklasse IC), während ein Echo bei allen anderen Empfängern vor der Therapie in Betracht gezogen werden sollte (Empfehlungsklasse IIaC). Ein höhergradiges CRS von Grad > 2 gemäß der ASTCT-Klassifikation sollte zu einer Neubewertung der genannten Parameter führen, und bei allen Patienten mit CRS ist eine frühzeitige Initiation von Glukokortikoiden und Anti-IL-6-Agenzien (z. B. Tocilizumab), die bei der Reduzierung von CRS-bedingten Nebenwirkungen hochwirksam sind, möglich.
Fazit
Der Einsatz von CAR-T-Zelltherapien kann schwerwiegende kardiovaskuläre Komplikationen mit sich bringen.
Deshalb ist eine intensive Überwachung der Patienten sinnvoll: mit Biomarker-Bestimmung, EKG und Echo.
Kontakt-- Prof. Dr. Matthias Totzeck, Universitätsklinikum Essen
Literatur-- 1. Mahmood SS et al. Eur Heart J. 2023; https://doi.org/10.1093/eurheartj/ehad117

