Medikamentöse Therapie des HI-bedingten kardiogenen Schocks
Herzinsuffizienz(HI)-Medikation-- Der kardiogene Schock (KS) ist ein komplexes Syndrom mit hoher Morbidität und Mortalität. Mehr als die Hälfte aller Fälle eines kardiogenen Schocks sind auf eine Herzinsuffizienz zurückzuführen (HI-KS). Die Katecholamin-Therapie fußt auf schwachen Daten und beginnt ab Stadium C.
Veröffentlicht:
Mechanische Kreislaufunterstützung soll bei Patienten im Stadium C–E erwogen werden. Kiryl Lis/stock.adobe.com
© Kiryl Lis/stock.adobe.com
Der kardiogene Schock (KS) ist ein heterogenes Syndrom mit hoher Morbidität und Mortalität. Kriterien zur Diagnose des KS schließen neben der Hypotonie (> 30 min) auch Zeichen der pulmonalen Stauung und der Minderperfusion von Endorganen (Oligurie, kalte Extremitäten, Bewusstseinsveränderungen, Laktat > 2 mmol/l) ein. Nach der Diagnosestellung sollten die Ursachen (Myokardinfarkt vs. Herzinsuffizienz), der ventrikuläre Phänotyp (linksventrikulärer, rechtsventrikulärer, biventrikulärer KS), die klinische Präsentation und der Schweregrad des Schocks identifiziert werden. Die SCAI-CSWG-Klassifikation unterscheidet fünf Schweregrade A–E und erlaubt eine Abschätzung der Krankenhaus(KH)-Mortalität, die je nach Stadium zwischen 10 % (Stadium B) und 60 % (Stadium E) liegt (Abb. 1).
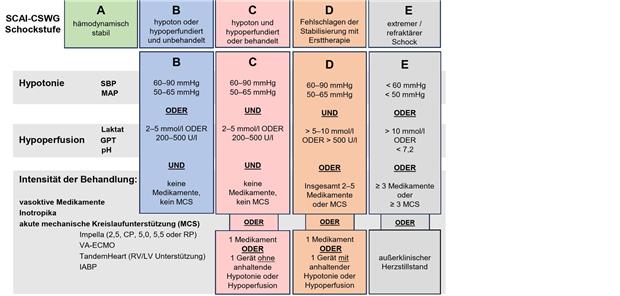
Parameter und Interventionen der SCAI-CSWG Schockstadien A–E (Abb. 1)-- Ausgewählte Parameter für Hypotonie, Hypoperfusion und Behandlungsintensität, abgeleitet von der Arbeitsgruppe für kardiogenen Schock (CSWG).modifiziert nach Kapur NK et al. JACC 2022:80(3):185-98GPT: Glutamat-Pyruvat-Transaminase, MAP: mittlerer arterieller Druck, SBP: systolischer Blutdruck, SCAI: Gesellschaft für kardiovaskuläre Angiografie und Interventionen, CSWG: Arbeitsgruppe Kardiogener Schock, LV: linker Ventrikel, RV: rechter Ventrikel, MCS: mechanische Kreislaufunterstützung, VA-ECMO: venoarterielle extrakorporale Membranoxygenierung, IABP: Intraaortale Ballonpumpe.
© Helbing
Datenlage zur medikamentösen Therapie ist unzureichend
Der Fokus in der Akutphase liegt auf der Stabilisierung des Patienten und dem Erhalt der Gewebeperfusion sowie der Verhinderung von Endorganschäden. Viele dieser Patienten sind gestaut und benötigen eine intravenöse Therapie mit einem Schleifendiuretikum (initial in der doppelten häuslichen oralen Dosis). Steigt die Urinausscheidung nicht adäquat an, sollte die Häufigkeit der Diuretika-Dosis erhöht werden und ggf. eine Dauerinfusion erfolgen. Bei therapierefraktärer Stauung kann das Schleifendiuretikum mit Hydrochlorothiazid oder Acetolamid kombiniert werden. Im Low-Output-Syndrom kann die zusätzliche Therapie mit Inotropika die pulmonale Stauung bessern, indem diese den Teufelskreis aus Minderperfusion, Stauung und Diuretikaresistenz durchbricht.
Charakterisierung der verschiedenen Schockstadien
Im beginnenden Schock (Stadium B) liegt entweder eine Hypotonie oder eine Hypoperfusion vor, die durch eine Lactat- und/oder GPT-Erhöhung charakterisiert ist. Dabei ist eine normotenisve Hypoperfusion ein unabhängiger Risikofaktor für die Mortalität im KS. Der KS im Stadium C ist durch eine Hypotonie mit Hypoperfusion gekennzeichnet (Abb. 1). Der Einsatz eines Pulmonaliskatheters (PAK) sollte in Betracht gezogen werden, um den ventrikulären Phänotyp zu charakterisieren und häufig auftretende klinische Verschlechterungen frühzeitig zu erkennen. Die derzeit laufende PACCS-Studie untersucht, ob PAK-gesteuertes Management die Mortalität des HI-KS reduziert. Neben einer Hypotonie und der Verminderung des Herzindex sind beim biventrikulären Phänotyp sowohl der PCWP als auch der rechtsatriale Druck erhöht. Ab Stadium C wird meist zur Stabilisierung eine vasoaktive/inotrope Substanz eingesetzt (Abb. 1). In den Stadien D–E nimmt die Behandlungsintensität weiter zu.
Katecholamine in der niedrigsten Dosis und so kurz wie nötig einsetzen
Häufig ist bei Hypotonie die Gabe eines Vasopressors bereits vor Beginn der inotropen Substanz erforderlich. Noradrenalin gilt als der Vasopressor der Wahl, da unter Adrenalin bzw. Dopamin die Mortalität erhöht war und Nebenwirkungen vermehrt auftraten. Dobutamin wird als Inotropikum der Wahl empfohlen. Jedoch können darunter Arrhythmien und Hypotonien auftreten. Bei fortgeschrittener HI war Dobutamin im Vergleich zu Placebo mit dem vermehrten Auftreten klinischer Ereignisse und einer erhöhten 6-Monats-Mortalität assoziiert. Bei Versagen von Dobutamin kann der Ca-Sensitizer Levosimendan eingesetzt werden. Im Vergleich zu Dobutamin kam es unter Levosimendan zu einer Reduktion der ICU-Aufenthaltsdauer sowie zur Besserung hämodynamischer Größen (CI, PCWP, MAP). Trotz günstiger Effekte konnte keine adäquat gepowerte Studie eine Reduktion der Mortalität unter Levosimendan zeigen. Um Hypotonien zu vermeiden, sollte vor Beginn der Volumenstatus optimiert und ggf. auf den initialen Levosimendan-Bolus verzichtet werden. Neben Hypotonien werden vermehrt Vorhofflimmern, Hypokaliämie und Kopfschmerzen beobachtet.
Die kombinierte Gabe von Levosimendan zur Firstline-Therapie mit Dobutamin-Noradrenalin zeigte in Metaanalysen günstige hämodynamische Effekte. Inwieweit Levosimendan zusätzlich zur Katecholamintherapie die Mortalität beeinflusst, wird derzeit in der LevoHeartShock-Phase-III-Studie untersucht. Die Phosphodiesterase-Hemmer Milrinon und Enoximon zeigten in großen Studien keinen Nutzen hinsichtlich Mortalität oder Hospitalisierungen bei Patienten mit fortgeschrittener oder akuter Herzinsuffizienz. Unter Milrinon stieg bei ischämischer Kardiomyopathie die KH-Mortalität und es wurden vermehrt Hypotonien und Arrhythmien beobachtet.
Die Therapieplanung sollte im interdisziplinären Schock-Team erfolgen
Bei Patienten im Stadium C–E, die sich unter initialer medikamentöser Therapie nicht bessern, sollte im Schock-Team ein Einsatz von mechanischen Unterstützungssystemen (MCS) erwogen werden. Einige MCS können temporär eingesetzt werden und erlauben die Erholung des Herzens (bridge to recovery) und anderer Organe wie Niere und Leber. Zusätzlich sollte auch ein Plan für Patienten erarbeitet werden, bei denen unter MCS-Therapie eine Erholung ausbleibt. Hierbei dient die temporäre MCS-Therapie als „bridge to decision“ für fortgeschrittene Therapien wie HTX und VAD.
Fazit
Bis heute existieren keine überzeugenden Daten, die eine Reduktion der Mortalität durch die medikamentöse Therapie mit spezifischen inotropen oder vasoaktiven Substanzen beim kardiogenen Schock belegen.
Angesichts der begrenzten Datenlage besteht ein großer Bedarf an RCT, um diese Lücken zu schließen und den Einfluss inotroper/vasoaktiver Substanzen im kardiogenen Schock zu ermitteln.
Literatur bei der Verfasserin und dem Verfasser
Kontakt-- PD Dr. Thomas Helbing, Zentrum für kardiovaskuläre Akutmedizin Mannheim (ZKAM), I. Medizinische Klinik, Universitätsmedizin Mannheim, thomas.helbing@umm.de

