Teil 1 einer Serie
Neue ESC-Leitlinie Onkokardiologie
Update-- Erst kürzlich wurden zum ersten Mal ESC-Leitlinien zur onkokardiologischen Versorgung herausgebracht. Sie liefern detaillierte Empfehlungen zur Risikobeurteilung vor Therapie, zur Diagnostik und zur Primärprävention bei Risikopatienten. Ein Überblick.
Veröffentlicht:
Viele Krebstherapien wirken kardiotoxisch.
© BURGER / PHANIE / Science Photo Library
Die Prävention kardiovaskulärer Nebenwirkungen ist ein essenzieller Bestandteil der onkokardiologischen Behandlung. Die 2022 veröffentlichten ESC-Leitlinien Kardioonkologie geben nun detaillierte Empfehlungen für die Risikobeurteilung vor Therapie, für geeignete diagnostische Maßnahmen und für Möglichkeiten zur Primärprävention bei Risikopatienten.

Dr. Lars Michel, Universitätsklinikum Essen
© Michel

Prof. Matthias Totzeck, Universitätsklinikum Essen
© Totzeck
Durch Minimieren kardiovaskulärer Nebenwirkungen über das gesamte Kontinuum der Behandlung wird Patienten die bestmögliche onkologische Therapie sicher ermöglicht. In einer Serie von Artikeln sollen die einzelnen Aspekte der Leitlinie in Hinblick auf die onkokardiologische Versorgung des wachsenden Kollektivs betroffener Patienten/Patientinnen gegeben werden [1].
Phasen der onkokardiologischenBehandlung
Die onkokardiologische Behandlung richtet sich nach der jeweiligen Phase der onkologischen Therapie, und lässt sich in vier Phasen unterteilen (Abb. 1). Die erste Phase besteht in der onkokardiologischen Erstvorstellung nach Diagnosestellung sowie Festlegung der geplanten Krebstherapie, aber noch vor Einleitung einer Therapie. Neben der Erstdiagnose kann eine erneute Vorstellung vor Therapiebeginn auch bei einer substanziellen Therapieumstellung erfolgen, wie es zum Beispiel im Falle eines Rezidivs der Krebserkrankung notwendig werden kann. Welche Patienten einer onkokardiologischen Vorstellung vor Therapiebeginn bedürfen, wie die Risikoerfassung abläuft und welche Konsequenzen sich für die weitere Therapie ableiten, wird im Folgenden erläutert.
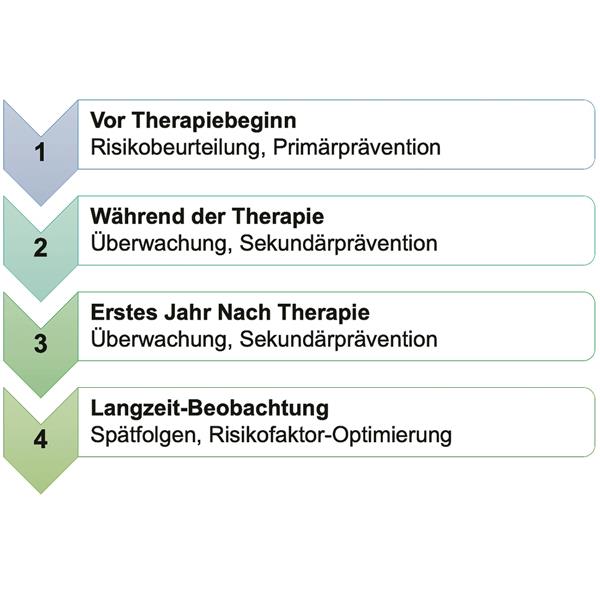
Abb. 1: Phasen der onkokardiologischen Behandlung.
© Michel/Trotzeck
Welcher Patient profitiert von einer onkokardiologischen Vorstellung?
Jeder Patient bedarf einer Risikoabschätzung für die Entwicklung einer Krebstherapie-assoziierten Kardiotoxizität vor Therapiebeginn (Klasse-IB-Empfehlung). Bei ca. 500.000 Krebsneuerkrankungen pro Jahr in Deutschland [2] ergibt sich zwangsläufig, dass die erste Risikoabschätzung durch die behandelnde Onkologie/Hämatologie erfolgt. Nur bei Patienten mit hoher oder sehr hoher Risikokonstellation und selektierten Patienten mit mittlerem Risiko wird eine dezidierte onkokardiologische Vorstellung empfohlen, wohingegen Patienten mit niedriger Risikokonstellation nur bei Anzeichen oder Symptomen einer kardiovaskulären Nebenwirkung in der onkologischen Weiterbetreuung einer onkokardiologischen Vorstellung bedürfen. Die Leitlinie betont, dass Niedrigrisikopatienten ohne Verzögerung einer Therapie zugeführt werden sollen (Klasse-IC-Empfehlung) [1].
Wie erfolgt die Risikobestimmung?
Die Risikobestimmung erfolgt auf Basis des therapieassoziierten Risikos sowie des individuellen, patientenassoziierten Risikos. Bei Patienten, welche bereits in der Vergangenheit eine Krebstherapie erhalten haben, kann das Risiko zusätzlich erhöht sein (Abb. 2).

Abb. 2: Risikofaktoren für die Entwicklung einer Krebstherapie-assoziierten Nebenwirkung.
© Michel/Trotzeck
Das klassische kardiovaskuläre Risikoprofil mit Erfassung von arterieller Hypertonie, Diabetes mellitus, Hypercholesterinämie und Nikotinabusus gilt als Risikofaktor für kardiovaskuläre Nebenwirkungen vieler Substanzklassen. Obwohl die Score-basierte Erfassung mittels des SCORE2 oder des SCORE2-OP der ESC-Leitlinien für kardiovaskuläre Prävention von 2021 [3] nicht für Krebspatienten validiert wurde, wird die Verwendung bei Patienten > 40 Jahren empfohlen. Patienten mit bestehender kardiovaskulärer Vorerkrankung benötigen eine dezidierte Erfassung der Art und Schwere der bestehenden Erkrankung, oft auch auf Basis weiterer diagnostischer Modalitäten wie einer Stress-Echokardiografie oder einer Computertomografie (CT)-Koronarangiografie.
Die Erfassung des therapieassoziierten Risikos basiert auf der Therapiemodalität, der Substanzklasse, der kumulativen Dosis sowie weiterer Modalitäten wie eine Kombinationstherapie der Applikationsart. Am Beispiel der Anthrazyklin-Chemotherapie lässt sich die Beurteilung des therapieassoziierten Risikos gut nachvollziehen. Eine Hochrisikokonstellation besteht bei einer kumulativen Dosis von 250 mg/m2 Doxorubicin-Äquivalent. Weitere Risikofaktoren sind eine vorangegangene Therapie mit Trastuzumab, eine weitere Chemotherapie oder eine thorakale Bestrahlung (Abb. 3) [4].
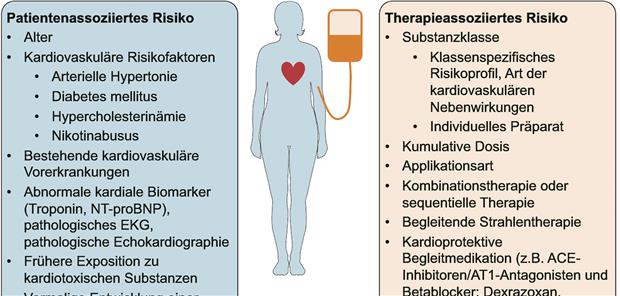
Abb. 3: Patienten- und therapieassoziierte Risikofaktoren. ACE-Inhibitor, Angiotensin-Converting-Enzym-Inhibitor; AT1-Antagonist, Angiotensin-II-Rezeptor Subtyp 1-Antagonist.
© Michel/Trotzeck
Die Heart Failure Association-International Cardio-Oncology Society (HFA-IC-OS) Basisrisiko-Tabelle bietet eine strukturierte Risikoeinteilung anhand definierter Variablen für die gebräuchlichsten Substanzklassen und sollte bei Patienten vor potenziell kardiotoxischer Chemotherapie in Betracht gezogen werden (Klasse-IIaC-Empfehlung). Der Score erfasst vorbestehende Erkrankungen, das kardiovaskuläre Risikoprofil, die linksventrikuläre Funktion und kardiale Biomarker (siehe unten) und kann durch die behandelnde Onkologie/Hämatologie ohne Notwendigkeit einer spezifischen onkokardiologischen Vorstellung erhoben werden [1].
Welche Diagnostik ist sinnvoll?
In der Basisdiagnostik vor Einleitung einer Krebstherapie kommen, abhängig von Risikoprofil und geplanter Therapie, das Ruhe-EKG, die transthorakale Echokardiografie (TTE) und die kardialen Biomarker Troponin sowie „N-terminales pro brain natriuretic peptide“ (NT-proBNP) zum Einsatz. Die kardiale Magnetresonanztomografie (MRT) kann bei spezifischen Fragestellungen als Zusatzdiagnostik zum Einsatz kommen. Die apparative Diagnostik vor Therapiebeginn dient nicht nur zur Erfassung bisher unentdeckter kardiovaskulärer Vorerkrankungen, sondern auch zur Festlegung von Basisparametern, um dann unter Therapie eine entsprechende Dynamik feststellen zu können.
Alle Patienten sollten vor der Krebstherapie ein 12-Kanal-EKG erhalten, da dieses als einfache und kostengünstige Methode eine Vielzahl von Rückschlüssen auf kardiovaskuläre Erkrankungen zulässt. Die Beurteilung der QTc-Zeit vor Therapiebeginn ist wichtig, da viele Substanzklassen eine Verlängerung der QTc-Zeit verursachen können.
Die TTE ist die primäre Modalität zur Evaluation der kardialen Funktion (Klasse-IC). Wann immer möglich sollte die dreidimensionale Analyse der linksventrikulären Ejektionsfraktion der zweidimensionalen Bestimmung vorgezogen werden. Bei jedem Patienten sollte der Global Longitudinal Strain quantifiziert werden, da dies für verbreitete Therapieformen, wie der Anthrazyklin-Chemotherapie, als Basis für die Definition einer Kardiotoxizität dient. Die kardiale MRT-Untersuchung ist speziellen Fragestellungen oder bei ungenügender Bildqualität in der TTE vorbehalten (Klasse IIbC). Die Bestimmung von Troponin und NT-proBNP wird bei allen Patienten empfohlen, die dem Risiko einer kardiovaskulären Nebenwirkung ausgesetzt werden. Es wird betont, dass die Bestimmung von Basismesswerten entscheidend für die weitere Überwachung unter Therapie ist, um eine Dynamik frühzeitig zu erkennen. Insbesondere für die Entwicklung einer linksventrikulären Dysfunktion unter Anthrazyklin-Chemotherapie oder Trastuzumab, für die Immuncheckpoint-Inhibitor-assoziierte Myokarditis und für das schwere „cytokine release syndrome“ bei Chimeric antigen receptor (CAR)-T-Zell-Therapie ist Troponin ein wichtiger Verlaufsparameter [5, 6].
Wie bespreche ich die Ergebnisse?
Die aktuellen ESC-Leitlinien Kardioonkologie betonen die Wichtigkeit einer guten Kommunikation mit betroffenen Patienten. Auf Basis der Risikostratifizierung soll Patienten der Zusammenhang zwischen kardiovaskulären Risikofaktoren und dem Risiko für die Entwicklung kardiovaskulärer Nebenwirkungen unter Krebstherapie erklärt werden. Durch Schaffung eines Bewusstseins soll eine Optimierung des kardiovaskulären Risikoprofils durch Behandlung modifizierbarer Faktoren und Lebensstiloptimierung erreicht werden. Gleichzeitig wird eine Adhärenz an die onkokardiologische Mitbehandlung auch im langfristigen Verlauf gefördert. Indem Patienten schon vor Therapiebeginn mögliche Symptome und Zeichen einer beginnenden kardiovaskulären Nebenwirkung erklärt werden, soll ein frühzeitiges Eingreifen ermöglicht werden [1].Fazit
Vor einer Krebstherapie sollte jeder Patient/jede Patientin bzgl. des Risikos für kardiovaskuläre Nebenwirkungen beurteilt werden.
Das Risiko für kardiovaskuläre Nebenwirkungen definiert sich durch patientenspezifische und therapiespezifische Risikofaktoren.
EKG, Echo und kardiale Biomarker bilden die Basis der Diagnostik.
Die adäquate Patientenkommunikation ist eine wichtige Säule der onkokardiologischen Behandlung.
Literatur--
1. Lyon AR et al. Eur Heart J. 2022; https://doi.org/10.1093/eurheartj/ehac244
2. Zentrum für Krebsregisterdaten 2022 ; https://www.krebsdaten.de/Krebs/DE/Content/Krebsarten/Krebs_gesamt/krebs_gesamt_node.html. Zugriff am 18.10.2022.
3. Visseren FLJ et al. Eur Heart J. 2021:42(34):3227-37, https://doi.org/10.1093/eurheartj/ehab484
4. Rassaf T et al. Clin Res Cardiol. 2021;109(10): 1197-222, https://doi.org/10.1007/s00392-020-01636-7
5. Michel L et al. Eur J Heart Fail. 2020;22(2):350-61, https://doi.org/10.1002/ejhf.1631
6. Totzeck et al. Eur Heart J. 2022;H43(20):1928-40, https://doi.org/10.1093/eurheartj/ehac106
wcms_BR
Kontakt-- Dr. Lars Michel, Prof. Matthias Totzeck, Klinik für Kardiologie und Angiologie, Westdeutsches Herz- und Gefäßzentrum, Universitätsklinikum Essen,

