Benötigen wir den HFA-PEFF-Score?
Diagnostik-- Um eine HFpEF zuverlässig zu diagnostizieren, reichen die bisherigen ESC-Kriterien nicht aus. Der HFA-PEFF-Score bringt die Diagnostik deutlich weiter. Dafür ist eine enge Verknüpfung von ambulantem und stationären Sektor hilfreich.
Veröffentlicht:
5 Punkte oder mehr? Dann ist die HFpEF sicher. everythingpossible/stock.adobe.com
© everythingpossible/stock.adobe.com
Bei der HFpEF handelt es sich im Vergleich zur HFrEF um ein multifaktorielles, von Komorbiditäten geprägtes Geschehen, das in seiner Gänze und Phänotypisierung nicht in allen Fällen vollständig verstanden ist. Entsprechend herausfordernd ist die Diagnostik. In den Anfangstagen beschränkte man sich lediglich auf die typische Klinik einer Herzinsuffizienz bei normaler systolischer LV-Funktion. Erstmalig wurden in den ESC-Leitlinien von 2016 genauere Diagnosekriterien, zusätzlich bestehend aus echokardiografischen Befunden und Biomarkern, formuliert [1]. Kliniker stehen im Alltag jedoch immer wieder vor der Herausforderung, dass Patienten Symptome angeben und nur ein Teil der von den Leitlinien geforderten Kombination echokardiografischer Kriterien und Biomarker vorliegt. Dies liegt sicherlich u. a. daran, dass alle diese Parameter in Ruhe erhoben werden. Die Symptomatik spielt sich bei HFpEF jedoch vor allem im Anfangsstadium bei Belastung ab.
Um diesem Problem Rechnung zu tragen, wurden zwei unterschiedliche Algorithmen vorgeschlagen. Zum einen wurde von B. Pieske und Mitarbeitern im Namen der HFA der ESC der HFA-PEFF-Score entwickelt [2]. Hier werden Punkte zunächst für bestimmte Kriterien verteilt (Tab. 1). Bei weniger als 1 Punkt ist das Vorliegen einer HFpEF unwahrscheinlich, bei ≥ 5 Punkten kann eine HFpEF als ausreichend gesichert angesehen werden. Für den Fall, dass der HFA-PEFF-Score in einem definierten Graubereich liegt (2–4 Punkte), sieht der Algorithmus einen Belastungstest mittels Stressechokardiografie oder (Belastungs-) Rechtsherzkatheteruntersuchung vor. Auch wurde nun erstmals eine ätiologische Abklärung der HFpEF gefordert, wie dies im aktuellen Update der Herzinsuffizienz-Leitlinien ebenfalls verlangt wird [3]. Der HFA-PEFF-Algorithmus erlaubt die prognoserelevante Diagnose auch für Patienten, bei denen nach bisher gültigen Kriterien der ESC-Leitlinien nicht die Diagnose einer HFpEF zu stellen wäre.
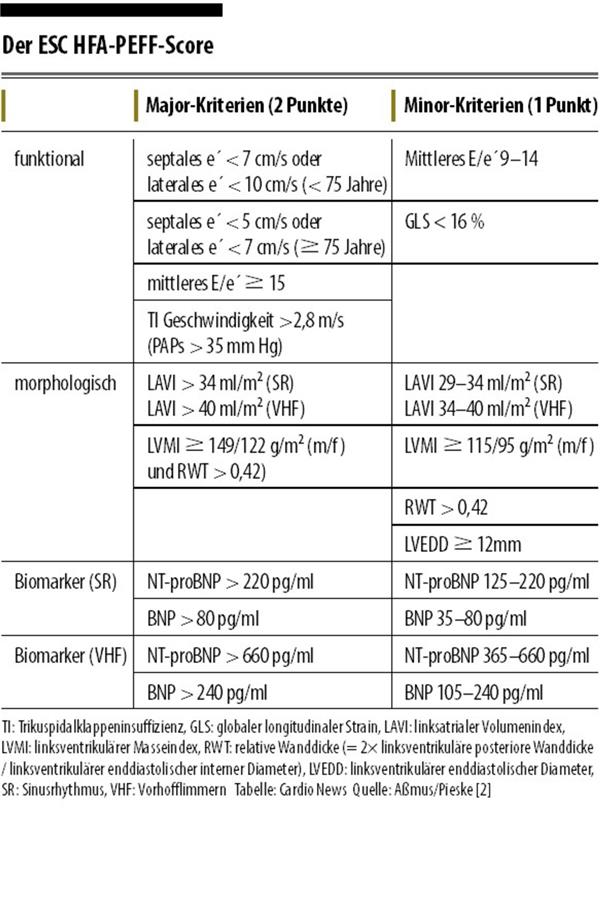
© Aßmus/Pieske
Beide Tests haben somit nachweislich eine prognostische Bedeutung für den Patienten. Bei begründetem Verdacht auf Herzinsuffizienz stellt sich jedoch mittlerweile mit der Empfehlung für die SGLT-2-Inhibitor-Therapie unabhängig von der LVEF oft die Frage, wie viel Diagnostik tatsächlich vor Verordnung dieser Substanzklasse erforderlich ist. Wir sind der Ansicht, dass eine korrekte Diagnostik der HFpEF zu fordern ist, jedoch sollte die notwendige Abklärung insbesondere auch der Ätiologie nicht der Therapieeinleitung mit einem SGLT-2-Inhibitor (Dapagliflozin oder Empagliflozin) im Weg stehen. Diese Therapie sollte aufgrund des schnellen Nutzens unverzüglich etabliert werden.
Für die erste Abklärung ist auch im ambulanten Setting eine orientierende Belastungsuntersuchung z. B. mittels Handgrip-Belastung im Echo möglich, und anhand der Veränderungen von E/e´ und des pulmonalarteriellen Drucks können sich hier erste Hinweise für oder gegen HFpEF ergeben. Für die detaillierte Abklärung ist gegenwärtig in unserem System eine gute Kooperation mit stationären Versorgern unverzichtbar, um eine Belastungsuntersuchung oder erweiterte Bildgebung zu ermöglichen. Hier erscheint uns vor allem die Zusammenarbeit innerhalb der Herzinsuffizienznetzwerke ein Weg zu sein, um auch überregional eine exakte HFpEF-Diagnostik und ätiologische Aufarbeitung zu erreichen. Für die Weiterentwicklung von Diagnostik und Therapie der HFpEF ist es essenziell, die Erkrankung ätiologisch exakt zu charakterisieren, so, wie es gegenwärtig – mit Limitationen – für die Amyloidose implementiert ist. Einen großen Fortschritt erwarten wir mit der herstellerübergreifenden einfachen Verfügbarkeit der Strain-Bildgebung, sowie durch die eines Tages hoffentlich vorhandene Möglichkeit von ambulanten Kardio-MRT-Untersuchungen, weil dann zahlreiche Differenzialdiagnosen (z. B. Fabry, Amyloidose, HCM) besser zu diagnostizieren sind.
Fazit
Der HFA-PEFF-Score ist für die Therapieeinleitung mit einem SGLT-2Inhibitor nicht erforderlich.
Ein Teil der HFpEF-Patienten ist jedoch nur über eine Belastungsuntersuchung korrekt zu identifizieren. Insofern sollte der Score bei uneindeutigen Fällen auch in der Routineversorgung zum Einsatz kommen.
Kontakt-- Prof. Dr. Birgit Aßmus, UKGM, Universitätsklinikum Gießen, birgit.assmus@innere.med.uni-giessen.de; Dr. Sebastian Köhler, Cardiocenter Ansbach, info@kardiologie-ansbach.de
Literatur--
1. Ponikowki P et al. Eur Heart J. 2016;37(27):2129-200
2. Pieske B et al. Eur Heart J. 2019;40:3297-317
3. McDonagh T et al. Eur Heart J. 2023; https://doi.org/10.1093/eurheartj/ehad195
4. Aizpurua AB et al. Eur J Heart Fail. 2020;22(3):413-21
5. Segar MW et al. Circulation. 2019;139:1851-3
6. Reddy YNV et al. Circulation. 2018;138:861-70

